Isabel Estruch Pons, María Serna Gandia, Daniel Paz Martín.
Referencia completa: Robinson S, Zincuk A, Strom T, Larsen TB, Rasmussen B, Toft P. Enoxaparin-effective dosage for intensive care patients: double-blinded, randomised clinical trial. Critical Care 2010.14:R41. (PubMed) (pdf)
Introducción
El paciente crítico está especialmente predispuesto a sufrir tromboembolismos por muy diversos factores: fallo cardíaco, traumatismos, sepsis, cáncer, edad avanzada, obesidad, inmovilización, ventilación mecánica, monitorización invasiva 1-5. La prevalencia de trombosis venosa profunda entre los pacientes que no reciben profilaxis se encuentra entre el 10-80% 1.
Objetivo
Determinar la dosis óptima de enoxaparina subcutánea capaz de alcanzar los mejores niveles de actividad Anti-Factor Xa (aFXa) en pacientes críticos.
Materiales y Métodos
Se realizó un estudio prospectivo, aleatorizado y doble ciego en la UCI médico-quirúrgica de 18 camas del Odense University Hospital (OUH) en Dinamarca, durante un periodo de tiempo de 3 años (febrero 2006 – Marzo 2009). Fueron reclutados 72 pacientes mayores de edad admitidos de forma consecutiva en la unidad, con una estancia mínima de 24 horas. Se excluyeron aquellos con peso menor de 50 kg. o mayor de 90 kg., con diátesis hemorrágica, embarazadas, los que necesitaron intervención quirúrgica durante el tiempo del estudio o los que requerían técnicas de HVVDFC.
Se les distribuyó en cuatro grupos según recibieran la dosis de 40 (grupo control) 50, 60 ó 70 mg. de enoxaparina subcutánea. La efectividad de la enoxaparina fue medida por la aFXA, considerándose niveles efectivos entre 0,1-0,3 UI/ml. 6, 8. Los pacientes se consideraron como no-respondedores si no había cambios en los niveles de aFXa después de la administración de enoxaparina.
Durante el día del estudio se tomaron muestras de sangre inmediatamente antes, a las 4, 12 y 24 horas después de la administración de la enoxaparina para determinar la variable primaria del estudio; actividad del aFXa y otras variables secundarias; Antitrombina, Tiempo de Protrombina, Tiempo de Tromboplastina Parcial Activada, Complejo Trombina-Antitrombina, Fibrinógeno, plaquetas, Dímero D, creatinina y aclaramiento de creatinina.
Resultados
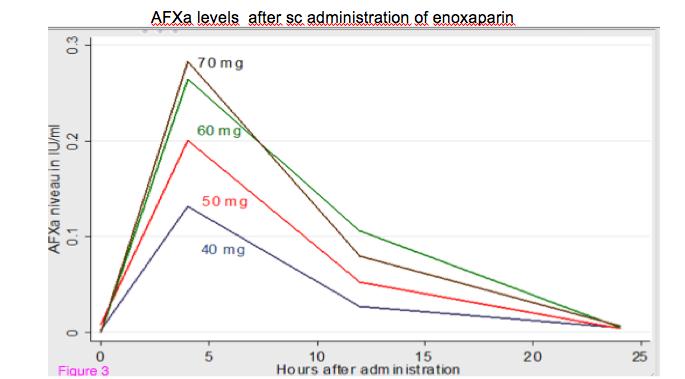
Se observó una correlación positiva entre la dosis de enoxaparina y los niveles de aFXa. El pico medio de aFXa, que ocurre a las cuatro horas de la administración, aumenta con la dosis siendo de 0,13 IU/ml., 0,14 UI/ml., 0,27 UI/ml. y 0,29 UI/ml. para 40, 50, 60 y 70 mg. respectivamente, con una diferencia estadísticamente significativa (p=0,002).
El grupo que recibió 40mg tuvo el mayor número de no respondedores (n=5) y se encontraron niveles subterapéuticos en un 28%, 67%, y 83% a las 4, 12 y 24 h. respectivamente.
Para la dosis de 60 mg. se encontraron niveles subterapéuticos en un 5%, 30% y 90% a las 4, 12 y 24 h respectivamente. Observándose en este grupo un efecto techo por encima del cual aparecían complicaciones hemorrágicas.
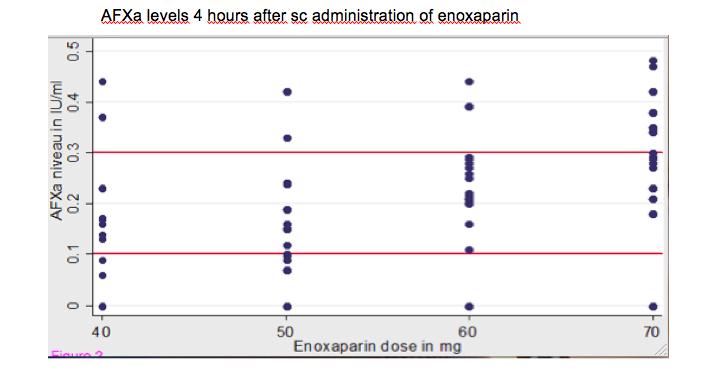
El grupo que recibió 70 mg. tuvo el mayor número de pacientes con aFXa > 0,3 UI/ml. (n=7). (Figuras 1 y 2)
No se encontraron diferencias significativas en las variables secundarias entre los cuatro grupos.
Comentario
Muchos y diversos mecanismos han sido propuestos por diferentes autores para explicar el grado de fracaso en la prevención del tromboembolismo del paciente critico, como la coadministración de agentes vasopresores 6, 7, 9, 10, la presencia de edema, la existencia de fallo multiorgánico, que podrían alteran la absorción, metabolismo y/o distribución de las heparinas 6.
Este estudio sugiere que la dosis insuficiente de enoxaparina podría ser en parte responsable del fracaso en la prevención de tromboembolismos, ya que confirma que el grupo de pacientes que recibió la dosis diaria standard de 40 mg. no alcanzaba niveles terapéuticos de aFXa.
Una limitación importante del estudio, es que éste no fue diseñado para determinar la presencia de trombosis venosa usando la técnica de referencia del ecodoppler y en su lugar se usaron los niveles de aFXa, eso a pesar de que numerosos estudios no encuentran relación directa entre aFXa y la actividad antitrombótica de la enoxaparina.
Además los pacientes fueron estudiados sólo durante un periodo de tiempo de 24 horas.
Otra limitación es que la enoxaparina dispensada por el equipo de enfermería se encontraba precargada en jeringas de 20 y 40 mg., lo que dificultaba la titulación de la dosis, y esto podría explicar en parte la variabilidad en los niveles de aFXa encontrados en pacientes del mismo grupo.
Además faltaría por determinar si los resultados obtenidos con enoxaparina se pueden extrapolar a otras HBPM.
De acuerdo con la crítica de Scholey et al. 11 otra limitación importante del estudio es la exclusión de pacientes con HVVFC, ya que en pacientes con alteración de la función renal la dosis diaria de enoxaparina 60mg podría producir un exceso importante de anticoagulación.
Además llama la atención que para conseguir una muestra de 72 pacientes consecutivos el periodo de tiempo necesario sea de 3 años (febrero 2006 – marzo 2009)
Son necesarios nuevos estudios para determinar si el aumento en los niveles de aFXa con dosis diarias de enoxaparina de 60mg se traduciría en menos fenómenos tromboembólicos sin aumento concomitante del riesgo de sangrado.
Bibliografía
1.- Geerts WH, Bergqvist D, Pineo GF et al. American College of Chest Physicians: Prevention of venous thromboembolism: American College of Chest Physicians Evidence-Based Clinical Practice Guidelines (8th Edition). Chest 2008, 133: 381S-453S. (PubMed) (pdf)
2.- Geerts W, Selby R: Prevention of venous thromboembolism in the ICU. Chest 2003, 124: 357S-363S. (PubMed) (pdf)
3.- Attia J, Ray JG, Cook DJ, Douketis J, Ginsberg JS, Geerts WH: Deep vein thrombosis and its prevention in critically ill adults. Arch Intern Med 2001, 161: 1268-1279. (PubMed) (full)
4.- Leizorovicz A, Mismetti P: Preventing venous thromboembolism in medical patients. Circulation 2004, 110: IV13-IV19. (PubMed) (pdf)
5.- Cook D, Douketis J, Meade M et al. Canadian Critical Care Trials Group: Venous thromboembolism and bleeding in critically ill patients with severe renal insufficiency receiving dalteparin thromboprophylaxis: prevalence, incidence and risk factors. Crit Care 2008, 12: R32. (PubMed) (pdf)
6.- Mayr AJ, Dí¼nser M, Jochberger S et al. Antifactor Xa activity in intensive care patients receiving thromboembolic prophylaxis with standard doses of enoxaparin. Thromb Res 2002, 105: 201-204. (PubMed)
7.- Dí¶rffler-Melly J, de Jonge E, Pont AC et al. Bioavailability of subcutaneous low-molecular-weight heparin to patients on vasopressors. Lancet 2002, 359: 849-850. (PubMed)
8.- Levine MN, Planes A, Hirsh J, Goodyear M, Vochelle N, Gent M: The relationship between anti-factor Xa level and clinical outcome in patients receiving enoxaparine low molecular weight heparin to prevent deep vein thrombosis after hip replacement. Thromb Haemost 1989, 62: 940-944. (PubMed)
9.- Cook D, Crowther M, Meade M et al. Deep venous thrombosis in medical-surgical critically ill patients: prevalence, incidence, and risk factors. Crit Care Med 2005, 33: 1565-1571. (PubMed)
10.- Rabbat CG, Cook DJ, Crowther MA et al. Dalteparin thromboprophylaxis for critically ill medical-surgical patients with renal insufficiency. J Crit Care 2005, 20: 357-363. (PubMed)
11.- Scholey GM, Saayman AG, Hingston DH, Wise MP: Renal function and thromboprophylaxis in critically ill patients. Critical Care 2010, 14:416. (PubMed) (pdf)
Isabel Estruch Pons. María Serna Gandia. Daniel Paz Martín . Servicio de Anestesiología y Cuidados Críticos. Hospital de Denia. Alicante.