José íngel Monsalve Naharro *. Manuel Gerónimo Pardo **. Ana María Rodilla Fiz ***.
Complejo Hospitalario Universitario de Albacete.
Introducción
Las nefrectomías por vía abierta son intervenciones agresivas que suelen ser realizadas con el paciente sometido a anestesia general, lo cual implica el empleo de ventilación mecánica y la aplicación de presiones positivas en la vía aérea. Sin embargo, el barotrauma asociado a la ventilación mecánica puede producir un neumotórax si el paciente presenta bullas pulmonares, por lo que en esta circunstancia concreta la relación beneficio-riesgo puede ser desfavorable a la anestesia general con ventilación mecánica y favorecer opciones menos habituales en las que el paciente mantenga la respiración espontánea 1-6.
Presentamos el caso de un paciente con bullas gigantes bilaterales que fue intervenido satisfactoriamente de nefrectomía abierta bajo anestesia epidural y sedación intravenosa, con preservación de la respiración espontánea.
Caso Clínico
El paciente que presentamos es un varón de 66 años, 70 kg. de peso y 168 cm. de altura (índice de Masa Corporal de 24,8), sin factores

predictores de vía aérea difícil. Era exfumador y seguía revisiones en consulta de neumología por enfisema bulloso con bullas gigantes bilaterales (Figuras 1 y 2) que condicionaban secundariamente obstrucción crónica al flujo aéreo. Fue diagnosticado de un tumor renal izquierdo y propuesto para una nefrectomía abierta programada.
A su ingreso en quirófano el paciente conocía que el plan inicial iba a ser intentar llevar a cabo el procedimiento bajo anestesia epidural y sedación, a lo cual accedió de buen grado. Se premedicó con 1 mg. de midazolam IV y fue monitorizado (pulsioximetría para saturación de oxígeno, presión arterial no invasiva, frecuencia cardíaca).
Se canalizó un catéter epidural posicionado entre L1 y L2, con el catéter insertado 4 cm. en sentido cefálico en el espacio epidural. Se administraron una dosis test de 3 mL. de bupivacaína 0,25% con adrenalina 1:200000 y, posteriormente, 5 mL. de ropivacaína 0,6%, con lo que se alcanzó un nivel sensitivo T6. En el intervalo de administración entre estos 2 bolos epidurales el propio paciente adoptó la posición de decúbito lateral derecho de modo que estuviese lo más confortable posible y, una vez en decúbito lateral, se iniciaron perfusiones IV de remifentanilo a dosis de 0,05 µg/kg/min y de propofol a 1 mg/kg/h, además de la infusión IV de analgesia preventiva (paracetamol 1 g. y metamizol 2 g.). También se administró aporte adicional de oxígeno mediante máscara facial al 40%.
Transcurridos unos 10 minutos del inicio de las perfusiones de remifentanilo y propofol el paciente estaba somnoliento y con los ojos cerrados, pero obedecía órdenes verbales simples y, al ser interrogado, refirió encontrarse tranquilo y confortable (nivel de sedación III en la escala de Ramsay), por lo que comenzó la intervención quirúrgica. Esta duró aproximadamente 90 minutos, transcurrió sin incidentes quirúrgicos, y los urólogos no refirieron encontrar especial dificultad para realizar la nefrectomía en ausencia de relajantes musculares (Figura 3).

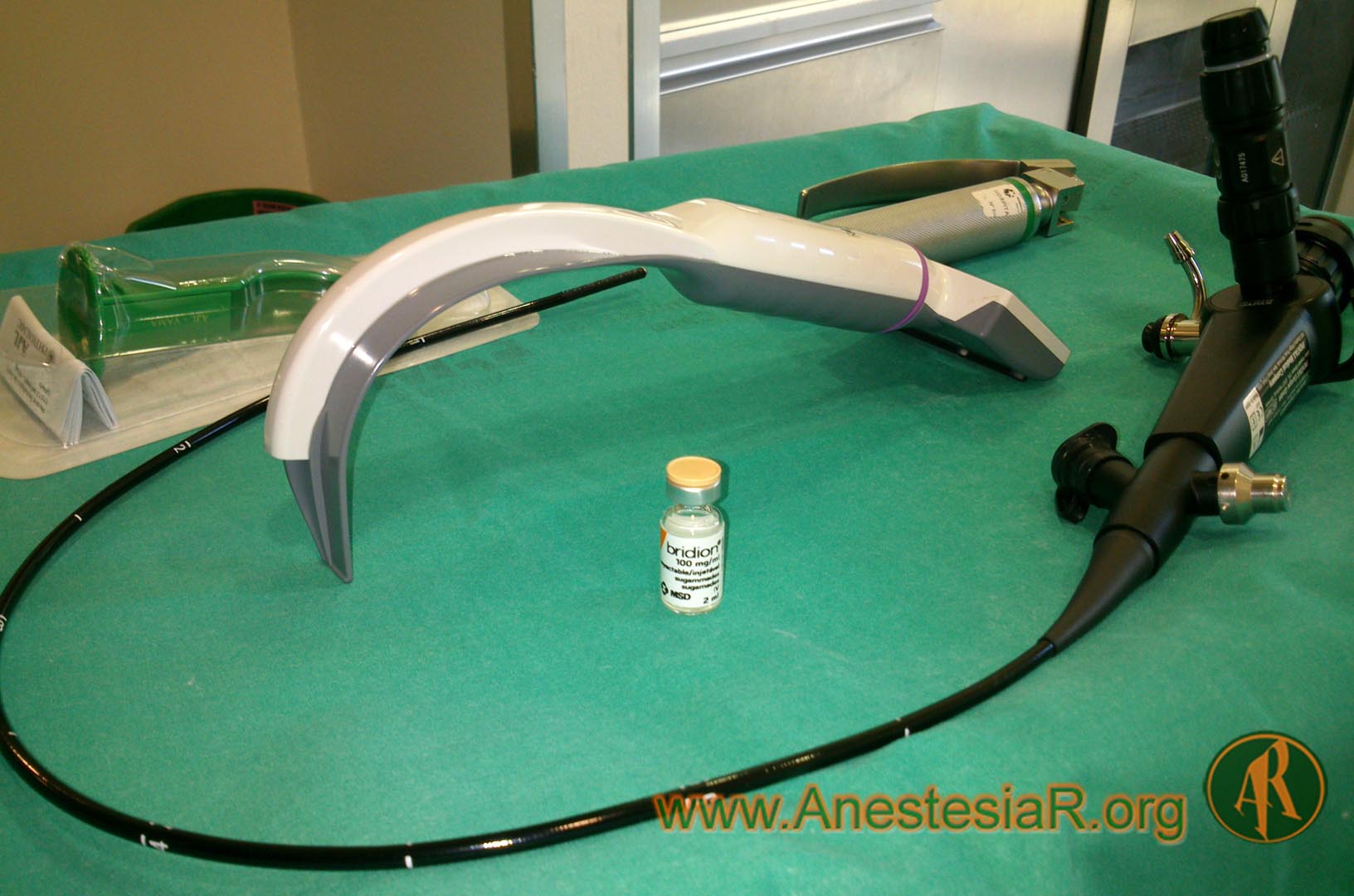
Durante todo este tiempo el paciente mantuvo el referido nivel de sedación, presentó estabilidad hemodinámica y conservó la respiración espontánea, manteniendo saturaciones de oxígeno medidas por pulsioximetría superiores a 95%. No obstante, durante todo el procedimiento anestésico-quirúrgico dispusimos de material para el abordaje de la vía aérea (diversos dispositivos supraglóticos y material habitual para intubación orotraqueal), y para el tratamiento de un eventual neumotórax (catéteres y tubos de drenaje torácico).
El postoperatorio inmediato cursó sin incidentes en la unidad de recuperación postanestésica, donde se inició analgesia mediante una perfusión continua epidural a 6 mL/h de una mezcla de levobupivacaína 0,125% y fentanilo 2 µg/mL.
Tras 2 horas de estancia fue dado de alta a la sala de hospitalización. Al alta de la unidad de recuperación refirió que el grado global de satisfacción había sido elevado.
Discusión
La nefrectomía abierta es una técnica quirúrgica que habitualmente se realiza bajo anestesia general, combinada o no con técnicas neuroaxiales, pero en este caso fue realizada bajo anestesia epidural con el apoyo de sedación. Esta actuación especial estuvo motivada por la patología pulmonar severa que presentaba el paciente descrito, pues nuestro principal objetivo en este paciente fue evitar las potenciales complicaciones de la ventilación mecánica (neumotórax, destete dificultoso, atelectasias, infecciones, etc.).
La primera de nuestras preocupaciones fue el temor a que se produjese un neumotórax por rotura de una bulla pulmonar. De hecho, esto condicionó la técnica anestésica, pues pretendíamos mantener al paciente en respiración espontánea para evitar las presiones positivas en la vía aérea, y para ello optamos por la anestesia epidural con apoyo de sedación. Este proceder ha sido empleado también con éxito en neurocirugía para resección de tumor intracraneal (asociando bloqueo del cuero cabelludo)6 e, incluso, en cirugía torácica mediante minitoracotomía para decorticación de la bulla (asociando epidural)3.
En el eventual caso de que el paciente no lo hubiese tolerado, el siguiente paso de nuestra estrategia habría sido la colocación de un dispositivo supraglótico con el objetivo de intentar profundizar el plano hipnótico pero preservando la respiración espontánea. Esta actuación también ha sido comunicada, en concreto en un paciente sometido a coagulación de hepatoma mediante microondas (asociando epidural)2, en otro para resección de tumor de codo (asociando plexo interescalénico)5, y para la realización de bypass coronario (asociando epidural)4. Incluso hay comunicado el caso de un paciente intervenido de aneurisma de la aorta abdominal que fue intubado orotraquealmente empleando succinilcolina como relajante muscular para posteriormente mantenerlo en respiración espontánea1.

Aparte de los 6 ejemplos mencionados (expuestos en orden de menor a mayor agresión sobre la vía aérea y, curiosamente, todos de origen asiático), no conocemos más comunicaciones de pacientes afectos de bullas pulmonares que hayan sido intervenidos bajo anestesia locorregional en respiración espontánea (con mayor o menor grado de sedación asociada).
Llegado el caso de que hubiésemos precisado el empleo de ventilación mecánica (por ejemplo porque los urólogos no hubiesen podido trabajar sin relajación muscular, o porque en las condiciones anteriormente referidas fuese imposible mantener unos niveles adecuados de saturación de oxígeno o de excreción de anhídrido carbónico), el riesgo de barotrauma y neumotórax habría sido importante.
Por este motivo habíamos preparado dispositivos de drenaje pleural, y nuestro plan consistía en evitar el empleo de óxido nitroso. En esta situación el empleo de tubos orotraqueales de doble luz es otra de las estrategias comunicadas en la literatura7, pero sólo funciona para bullas unilaterales y, por tanto, era inútil para nuestro paciente, puesto que tenía bullas bilaterales.
Finalmente, y por analizar a priori exhaustivamente todas las posibilidades teóricas, desestimamos por completo la colocación de tubos de drenaje pleural preoperatorios profilácticos, pues el balance beneficio-riesgo de esta actuación agresiva nos pareció desfavorable. No conocemos de ninguna comunicación sobre este aspecto en la literatura de cirugía extratorácica realizada a pacientes portadores de bullas.
Además del enfisema bulloso, el paciente comunicado presentaba obstrucción al flujo aéreo, y es conocido que este tipo de pacientes tienen un riesgo mayor que la población general8 de desarrollar otro tipo de complicaciones respiratorias cuando son sometidos a anestesia general, como empeoramiento de la insuficiencia respiratoria, o aparición de atelectasias o neumonías9,10, especialmente si la intervención quirúrgica es abdominal8. En estas situaciones se conoce que la analgesia epidural proporciona mejor control del dolor en cirugía mayor abdominal que los opioides sistémicos y puede reducir las complicaciones pulmonares postoperatorias8.
En este contexto, la anestesia epidural puede ofrecer ventajas con respecto a la anestesia general en pacientes con enfermedad pulmonar obstructiva crónica en estadios avanzados, mejorando la dinámica respiratoria (al evitar la curarización, los fármacos depresores respiratorios y con un mejor control analgésico postoperatorio), y mediante el mantenimiento de la ventilación espontánea al evitar las complicaciones derivadas de la instrumentación de la vía aérea y de la ventilación mecánica, como neumotórax (especialmente en nuestro caso), atelectasias, o destete prolongado. De hecho, se han reportado en la literatura numerosos casos de pacientes con patología pulmonar severa sometidos a cirugía abdominal mayor bajo anestesia neuroaxial preservando la respiración espontánea, como por ejemplo en cirugía de estómago11, colon12-13 y colecistectomías14,15.
Sin embargo, hasta la fecha han sido documentados pocos casos de anestesia epidural como técnica anestésica única para la realización de nefrectomías16,17. A finales de los años 90 se publicaron algunos casos de anestesia epidural para nefrectomías en pacientes donantes vivos con el objetivo de disminuir el dolor postoperatorio18. Haberal et al19 presentó una descripción de 20 intervenciones de este tipo realizadas bajo anestesia combinada intradural-epidural, observándola segura en procedimientos largos, con adecuado bloqueo motor para los cirujanos y con una analgesia postoperatoria y un grado de satisfacción de los pacientes adecuado20-22.
Conclusiones
La anestesia epidural asociada a sedación conservando la respiración espontánea constituye una valiosa alternativa a la anestesia general con ventilación mecánica en pacientes con enfermedades pulmonares severas que van a ser intervenidos de nefrectomía abierta.
Bibliografía
1.- Iwakura H, Kishimotot T, Takatori T, Koh J, Nakamura Y, Kosaka Y. Anesthetic management of a patient with abdominal aortic aneurysm (AAA) with giant bulla. Masui 1994;43(1):116-118. (PubMed)
2.- Nozaki K, Endou A, Sakurai K, Takahata O, Iwasaki H. Anesthetic management of a patient with a giant bulla and liver cirrhosis using a laryngeal mask airway and epidural analgesia. Masui 2001;50(6):639-641. (PubMed)
3.- Yen CR, Tsou MY, Lin SM, Chan KH, Chu YC. Thoracic anesthesia for a polymyositis patient undergoing awake mini-thoracotomy and unroofing of a huge pulmonary bulla. Acta Anaesthesiol Taiwan 2008;46(1):42-45. (PubMed)
4.- Suga K, Yoshida A, Kamada T, takao R, Kaneko T, Kobayashi Y. Respiratory management for a patient with a giant bulla and pulmonary dysfunction during off-pump coronary artery bypass grafting. Masui 2010;59(2):216-219. (PubMed)
5.- Sugiura T, Akiyoshi R, Kato R, Sasano H, Sobue K. Interscalene block combined with general anesthesia under spontaneous breathing in a patient with a giant bulla. Masui 2011;60(9):1101-1103. (PubMed)
6.- Kamath S, Bhadrinarayan V, Ranjan M, Umamaheswara Rao GS. Alternative approach for the anesthetic management of a patient with large pulmonary bulla presenting with an intracranial tumor for surgery. J Anesthesiol Clin Pharmacol 2012;28(2):272-273. (PubMed) (pdf1) (html)
7.- Caseby NG. Anaesthesia for the patient with a coincidental giant lung bulla: a case report. Can Anaesth Soc J 1981;28(3):272-276. (PubMed)
8.- Van Lier F, van der Geest PJ, Hoeks SE, van Gestel YR, Hol JW, Sin DD, et al. Epidural analgesia is associated with improved health outcomes of surgical patients with chronic obstructive pulmonary disease. Anesthesiology 2011;115(2):315-321. (PubMed) (pdf)
9.- Seigne PW, Hartigan PM, Body SC. Anesthetic considerations for patients with severe emphysematous lung disease. Int Anesthesiol Clin 2000;38(1):1-23. (PubMed)
10.- Edrich T, Sadovnikoff N. Anesthesia for patients with severe chronic obstructive pulmonary disease. Curr Opin Anaesthesiol 2010;23(1):18-24. (PubMed)
11.- Usukura A, Tsubokawa T, Yamamoto K. Anesthetic management of a patient with severe combined pulmonary disease under epidural anesthesia with spontaneous respiration. Masui 2008;57(5):624-627. (PubMed)
12.- Morton G, Bowler I. Combined spinal-epidural as an alternative method of anaesthesia for a sigmoid-colectomy. Anaesthesia 2001;56(8):815-816. (PubMed)
13.- Kapala M, Meterissian S, Schricker T. Neuraxial anesthesia and intraoperative bilevel positive airway pressure in a patient with severe chronic obstructive pulmonary disease and obstructive sleep apnea undergoing elective sigmoid resection. Reg Anesth Pain Med 2009;34(1):69-71. (PubMed)
14.- Cortiñas Sáenz M, Jiménez Vizuete JM, Vega Pérez F, Rubio González MV, Peyró García R, Cuesta Tobarra J. Colecistectomía abierta bajo anestesia epidural torácica en enfermedades intersticiales difusas del pulmón. Rev Esp Anestesiol Reanim 2004;51(3):164-167. (PubMed)
15.- Muñoz Rosado G, Alamán Orbañanos B, Moro Velasco C, García Porras R. Colecistectomía abierta bajo anestesia epidural torácica en pacientes con enfermedad pulmonar severa. Rev Esp Anestesiol Reanim 2008;55(10):648-650. (PubMed)
16.- Buzzetti V, Dellino E, Veschi G, Aveni MR, Quarenghi E. Nephrectomy in pulmonary tuberculosis patients: an anesthesiological approach. Arch Ital Urol Nefrol Androl 1991;63(3):351-354. (PubMed)
17.- Johnson TV, Bond N, Master VA. Radical nephrectomy via epidural-only anesthesia. Can J Urol 2010;17(5):5401-5402. (PubMed)
18.- Akpek E, Kayhan Z, Kaya H, Candan S, Haberal M. Epidural anesthesia for renal transplantation: a preliminary report. Transplant Proc 1999;31(8):3149-3150. (PubMed)
19.- Haberal M, EmiroÄŸlu R, Arslan G, Apek E, Karakayali H, Bilgin N. Living-donor nephrectomy under combined spinal-epidural anesthesia. Transplant Proc 2002;34(6):2448-2449. (PubMed)
20.- Akpek EA, Kayhan Z, Dí¶nmez A, Moray G, Arslan G. Early postoperative renal function following renal transplantation surgery: effect of anesthetic technique. J Anesth 2002;16(2):114-118. (PubMed)
21.- Sener M, Torgay A, Akpek E, Colak T, Karakayali H, Arslan G, et al. Regional versus general anesthesia for donor nephrectomy: effects on graft function. Transplant Proc 2004;36(10):2954-2958. (PubMed)
22.- Sener M, Torgay A, Akpek E, Aktas A, Colak T, Karakayali H, et al. The effect of anesthetic technique on early postoperative renal function after donor nephrectomy: a preliminary report. Transplant Proc 2005;37(5):2023-2027. (PubMed)
Especialista en Anestesiología y Reanimación.
Complejo Hospitalario Universitario de Albacete.
** Manuel Gerónimo Pardo.
Doctor en Medicina.
Especialista en Farmacología Clínica.
Especialista en Anestesiología y Reanimación.
Complejo Hospitalario Universitario de Albacete.
*** Ana María Rodilla Fiz.
MIR en Anestesiología y Reanimación.
Complejo Hospitalario Universitario de Albacete.



Estimados compañeros.
El caso me parece interesante y casi heroico pero me gustaria añadir una seria de puntualizaciones:
1-Colocar un drenaje de torax de de forma profilactico no es que no este indicado sino que es una gran yatrogenia, romper una bulla enfisematosa es fistula broncopleural asegurada,depedencia de un tubo de torax casi para siempre en ese paciente y pleurodesis la cual dudo tambien sea eficaz.
2-Obviamente hay que preparar la via aerea pero si este paciente se pone hipoxemico dentro de quirofano,¿como diagnostican el neumotorax?,el paciente si se pone hipoxemico pero la causa no tiene que ser neumotorax y a la auscultacioncon esas bullas me parece poco sensible e inespecifica.Pues como se haga una toraconcentesis de un bulla ocurre lo que he cometado antes, es una catastrofe.
3-Propongo, si se realiza anestesia locorregional, ademas del kit de via aérea, la sonda lineal de un eco portatil da el diagnostico inmediato de neumotorax y del sitio mas adecuado para pinchar.Ademas es facil de aprender.
4-No estaria de mas tampoco avisar a la Reanimacion/UCI pues un neumotorax a tension en estos pacientes suele ser una catastrofe hemodinamica.
Felicidades por la presentación del caso porque me parece muy bien documentado.