Belén Cobo García
Hospital Universitario Fundación de Alcorcón. Madrid
Introducción
La inducción de secuencia rápida (ISR) y la intubación despierto son técnicas anestésicas habituales en la inducción de pacientes con riesgo de aspiración pulmonar (AP) de contenido gástrico. Muchos de estos pacientes portan una sonda de forma previa a la inducción, generalmente nasogástrica (SNG) (1,2). No hay guías clínicas ni ensayos clínicos randomizados que aborden el manejo de la SNG durante la inducción, qué pacientes deben portar SNG, así como si es preferible mantenerla, retirarla al esófago o del todo antes de la inducción. Hay estudios prospectivos de la incidencia de reflujo gastroesofágico (RGE) en distintos grupos de pacientes con SNG durante la inducción (2).
Con todo ello, y valorando la experiencia clínica de diversos autores, se propone un algoritmo de manejo de la vía aérea (VA) en pacientes con riesgo de AP debido a la presencia de lesiones esofágicas, RGE o distensión gástrica para ayudar en la decisión del manejo de la SNG.
Revisión histórica
1.- Tipos de sondas de drenaje gástrico:
Hay referencias de empleo de sondas de drenaje gástrico (SDG) hace 400 años para alimentar o realizar lavados gástricos tras envenenamientos. En 1921 se diseñó la sonda de Levin de una luz para alimentación y drenaje gástrico. En 1934 Miller y Abbott diseñan una sonda de doble luz, con un balón en la punta para evitar la regurgitación gástrica. Su objetivo era prevenir el RGE mediante el inflado del manguito en la unión GE. Pronto esta técnica encontró dificultades para mantener un buen sellado sin producir daño local.
La sonda de Salem-Sump se introdujo en la década de los 60 como una sonda de doble luz con tubo de drenaje gástrico y un tubo menor secundario abierto a la atmosfera para permitir paso de aire y evitar daño en la mucosa durante la aspiración. De la goma inicial se pasó al poliuretano y la silicona. En la actualidad las sondas disponen de marcadores radiopacos y los tamaños entre 14 y 20 F son los empleados en adultos.
Se insertan por boca o nariz dependiendo del estado de alerta del paciente, si está intubado, presenta lesión nasal y de si se necesitara en el postoperatorio.
2.- Indicacion de la SNG:
Desde los años 30 fue habitual la descompresión gástrica en la cirugía abdominal para prevenir la AP, fuga por anastomosis o dehiscencia de suturas. Esta práctica se relacionó con disminución de la distensión abdominal y de vómitos postoperatorios.
Pero, por otro lado, la SNG se relacionó con persistencia de íleo postoperatorio y su sola presencia se asoció a RGE. Además, su empleo no estaba exento de complicaciones como tos, nausea, vómitos (con mayor riesgo de aspiración y alteración hemodinámica), colocación endobronquial, intracraneal o en oído medio, sangrado, ulceración, perforación, etc. Por ello, la decisión de colocar una SNG debe realizarse según criterios establecidos.
3.- Prevención del RGE en la era Pre-Sellick:
Se utilizaban diversas técnicas:
– Anestesia regional (principalmente la anestesia espinal alta).
– Intubación orotraqueal despierto con laringoscopia directa o intubación nasal ciega en respiración espontánea.
– Inducción inhalatoria con hiperventilación para prevenir los episodios de apnea y espasmo respiratorio que precedían al vómito.
– Inducción intravenosa y relajación en posición semisentada-40º. Asumía que la presión máxima intragástrica en el paciente relajado es de 18cm de H2O; la posición semisentada a 40º eleva en el paciente adulto la laringe unos 19 cm sobre la unión GE, por lo que el contenido gástrico no podría alcanzar la laringe.
– Otras técnicas: Retrasar la cirugía, vaciar el contenido gástrico con sonda y fármacos eméticos pre-inducción como la apomorfina.
La colocación de la SNG de forma previa a la cirugía y el mantenimiento de la misma durante la inducción fue la práctica más habitual.
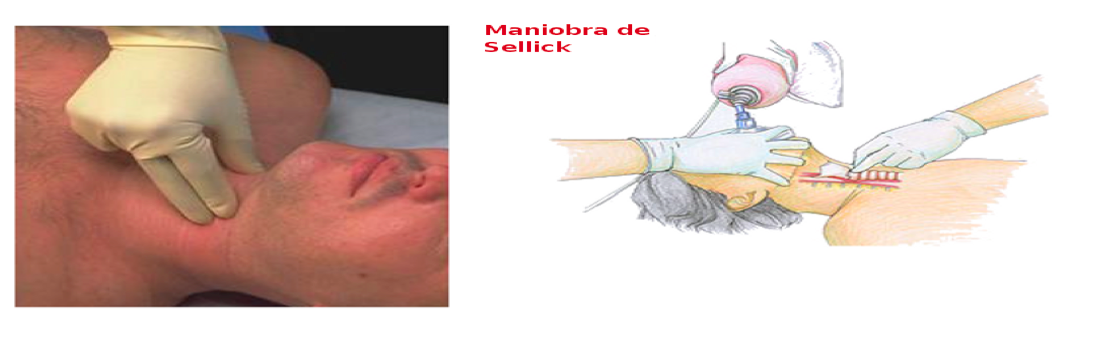
4.- La maniobra de presión cricoidea de Sellick:
Sellick (1) propuso la maniobra de presión cricoidea (PC) en 1961 para la prevención del RGE y la AP. Consistía en la oclusión del esófago superior por presión manual en dirección posterior sobre el cartílago cricoides (CC), demostrando que la PC obliteraba la luz esofágica a nivel de la 5ª vértebra cervical.
Sellick señaló inicialmente que era prudente primero descomprimir el contenido gástrico con una SNG, aunque nunca habría un completo vaciado, y después retiraba la sonda antes de inducir, ya que pensaba que la SNG aumentaba el riesgo de AP e impedía el sellado del esfínter esofágico inferior (EEI) y del esfínter esofágico superior (EES). Tras la inducción reintroducía la SNG.
Posteriormente, Sellick modificó su maniobra y mantuvo la SNG en la inducción, incluso las sondas de polivinilo no compresibles, con la maniobra de PC. Si se producía aumento de la PIG durante la inducción, la SNG permitía la salida del contenido gástrico mientras la PC evitaba la aspiración.
La maniobra de PC de Sellick fue incluida en el protocolo de ISR y su uso se extendió rápidamente en procedimientos quirúrgicos urgentes y electivos de pacientes con riesgo de AP (4).
5.- Situación actual:
En las últimas 2 décadas se ha cuestionado la eficacia de la PC (2,4,5) y ha propuesto abandonar su empleo porque:
a) su efectividad se había demostrado en cadáveres,
b) el esófago no está exactamente posterior al CC y puede no comprimirse en su totalidad,
c) la PC induce produce relajación del EEI,
d) la PC puede dificultar la ventilación, la intubación orotraqueal y colocación de mascarillas laríngeas,
e) puede inducir nausea y vómito,
f) hay casos descritos de AP a pesar de una maniobra de Sellick correcta.
Los estudios de Vanner and Pryle (6) con resonancia nuclear magnética mostraron que cuando 2 estructuras convexas como el CC y el cuerpo vertebral se presionan, sólo una parte del esófago se presiona entre ellos. Un ligero movimiento lateral del CC permite al resto del esófago presionarse contra el músculo largo del cuello que se extiende lateral al cuerpo vertebral, la sonda es desplazada y tiende a ocupar la parte de la luz menos comprimida. Estas observaciones sugieren que la SNG no interfiere con la compresión del EES durante la maniobra de Sellick y que incluso puede mejorarl
A pesar de esta evidencia de la efectividad de la PC en ocluir el esófago alrededor de la SNG, la visión primaria de Sellick se ha perpetuado y muchos autores han seguido recomendando retirar la SNG previamente a la inducción (2,4,5).
MANEJO DE LA VA EN PACIENTES CON RIESGO DE ASPIRACIÓN Y PAPEL ACTUAL DE LA SNG
Tras revisar la información disponible, se propone un algoritmo para el manejo de la VA en pacientes lesiones esofágicas, RGE y distensión gástrica, incluyendo las indicaciones de utilización de la SNG.
Los pacientes deberán ser preoxigenados de forma óptima (objetivo ETO2 > 90%) y se dispondrán medios para suministrar O2 suplementario durante el manejo de la VA.
1.- Lesiones esofágicas
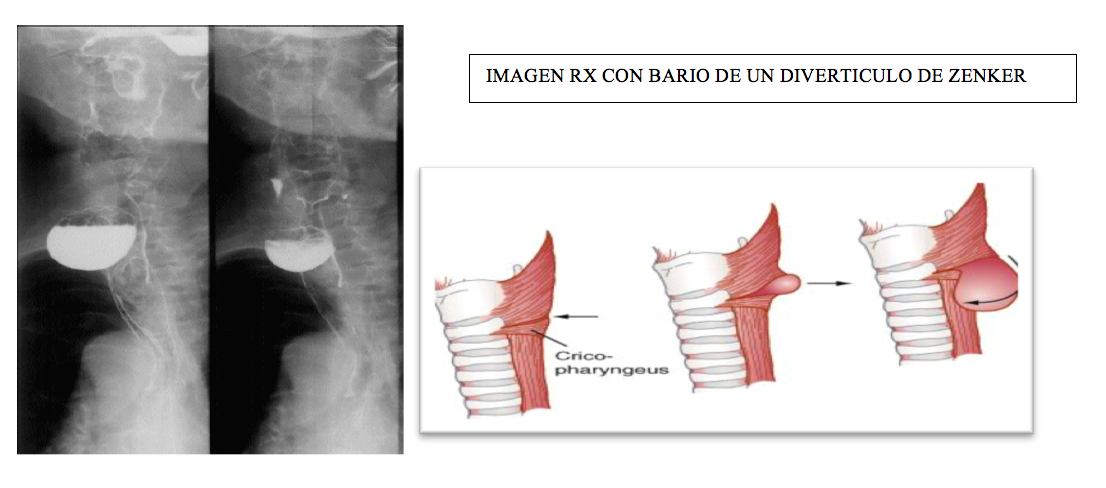
1.1.- Divertículo de Zenker:
Es un divertículo localizado en la parte superior del músculo cricofaríngeo por encima del EES, en un área débil (dehiscencia de Killian). La regurgitación de su contenido puede producirse en la inducción, intubación o incluso después, por filtración durante la cirugía.
Se debe intentar vaciar el contenido del saco por presión externa previamente a la inducción. Si el saco es pequeño estará posterior al CC y entonces la PC derramará su contenido en la faringe; si el saco es grande la PC presionará el cuello del saco y no se derramará. Por todo ello, el tránsito con bario determinará si es segura o no la maniobra de ISR. Otras alternativas son la intubación despierto y el empleo de bloqueo del plexo cervical superficial y profundo.
Se evitará toda maniobra que provoque arcada o induzca la regurgitación del contenido del divertículo. El manguito del tubo se inflará inmediatamente para evitar la filtración de fluidos.
No se debe introducir ninguna sonda, ya que puede perforar el divertículo.
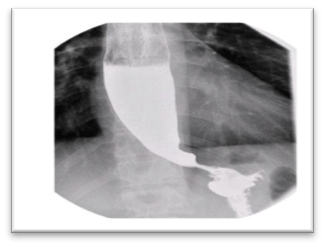
1.2.- Acalasia:
Trastorno idiopático del esófago caracterizado por disminución del peristaltismo y de la relajación del EEI, resultando en dilatación esofágica y retención de contenido alimenticio mezclado con aire. Se produce regurgitación, aspiración, infecciones respiratorias, obstrucción respiratoria superior compresión traqueal y obstrucción súbita del tubo durante la anestesia.
Su tratamiento es dilatación endoscópica del EEI, miomectomía o inyección de toxina botulínica.
Se debe intentar aspirar el máximo de contenido retenido mediante una sonda de gran calibre de forma previa a la anestesia.
Como técnica anestésica se recomienda la ISR o la intubación despierto.
2.- Reflujo gastroesofágico (RGE)
2 mecanismos fisiológicos protegen del RGE: la unión gastroesofágica y el esfínter esofágico superior (EES).
2.1.- Unión gastroesofágica:
La presión intragástrica (PIG) es 10-15 cm .de H2O superior a la esofágica. El mecanismo antirreflujo más importante es el tono del EEI, que mantiene una presión superior a la PIGo“ barrera de presión“.
La PIG aumenta por incremento de la presión intra abdominal o del volumen contenido en el estómago. Este aumento de la PIG se acompaña de un aumento adaptativo del tono del EEI.
En pacientes con síntomas de RGE o hernia de hiato hay disfunción del EEI que determina una menor“ barrera de presión“ y permite el reflujo del contenido gástrico. Estos pacientes deben recibir tratamiento farmacológico previo a la inducción para promover el vaciado gástrico, aumentar la barrera de presión o neutralizar el contenido gástrico.
La succinilcolina aumenta la PIG pero produce un aumento mayor de la presión en el EEI por lo cual el reflujo no se suele producir; sin embargo, este fenómeno está ausente en pacientes con RGE y distensión gástrica.
2.2.- Esfínter esofágico superior EES:
El tono del EES es de 38 mm de Hg en el paciente despierto, pero disminuye bruscamente por los relajantes e hipnóticos (excepto la ketamina), facilitando el RGE. La maniobra de PC suple la pérdida de tono del EES durante la inducción y relajación.
Se deben evitar las maniobras que aumentan el RGE cómo la obstrucción de la VA, esfuerzos respiratorios diafragmáticos que aumenten la PIG o ventilación con P. positiva superior a 20 cm. de H2O que induce aperturas intermitentes del EEI y del EES e insuflación gástrica.
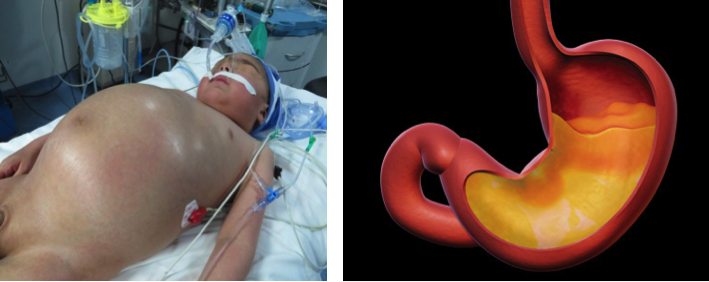
3.- Distensión gástrica (DG)
La obstrucción gástrica mecánica (estenosis pilórica), o funcional (íleo), produce distensión gástrica y aumento de PIG, RGE y vómito. La valoración del grado de distensión es clínica y radiológica. Un volumen estimado superior a 200 -300 ml. sugiere DG y es indicación de SNG.
El vaciamiento gástrico con SNG suele ser siempre incompleto, y depende del tamaño, tipo, correcta colocación, así como de la consistencia del contenido. Las sondas más efectivas son de gran calibre, multiperforadas y ventiladas o de doble canal.
Se recomienda adecuada selección, lubricación de la SNG y colocarla tragando o flexionando el cuello en el paciente despierto y en el enfermo dormido ayudarse de los dedos en la faringe, el fiador, laringoscopio o pinzas Magill. La comprobación, será radiológica y en su defecto clínica, con auscultación, inspección, valoración del aspecto y PH del aspirado, visualización directa con laringoscopia y comprobación de ausencia de capnografía.
Una vez aspirado el contenido gástrico y conseguida la menor PIG se realizará la inducción anestésica con PC. La SNG no se retirará durante la inducción y se conectará a aspiración durante la misma.
PECULIARIDADES DEL PACIENTE PEDIíTRICO
Los principios generales del manejo de la VA expuestos en el adulto son aplicables al niño. Sin embargo, presentan peculiaridades anatómicas, fisiológicas y malformaciones congénitas.
El niño durante el primer mes de vida presenta menor tono del EEI, produciéndose RGE fisiológico. También presentan RGE los niños intervenidos de atresia esofágica o gastrostomía y los niños con tetraparesia espástica, daño cerebral, trisomías, alteración laríngea o parálisis de las cuerdas vocales. Se recomienda tratamiento con funduplicatura en casos graves.
La ventilación con mascarilla facial induce gran distensión gástrica si hay obstrucción de la VA o se utilizan presiones >de 20 cm. H2O. El bloqueo neuromuscular produce parálisis del EES y DG por acúmulo de gas, lo cual aumenta el RGE. Por ello, se recomienda insertar una sonda gástrica tras la inducción, aspirar y retirarla finalmente antes de extubar.
1.- Estenosis congénita del píloro (ECP)
Es fundamental el meticuloso vaciado gástrico preoperatorio para reducir el riesgo de aspiración en la inducción. La SNG debe mantenerse durante la inducción y la cirugía. No hay evidencia de una técnica anestésica superior, siendo la inducción inhalatoria la más utilizada.
Se recomienda para el diagnóstico de la ECP el uso de ecografía (para evitar ingestión de contraste) o en su defecto utilizar contrastes solubles en agua.
2.- Atresia esofágica con fístula traqueoesofágica
Es la más común de las de las anomalías congénitas esofágicas.
La SNG se coloca preoperatoriamente y se realiza inducción inhalatoria o intravenosa. Se puede producir distensión gástrica severa por la ventilación con presión positiva, que puede inducir rotura gástrica o paro cardiaco. Para evitarlo se debe colocar el tubo endotraqueal distal a la fístula o realizar gastrostomía previa con anestesia local. También se puede emplear un catéter Fogarty para ocluir la fistula y realizar la cirugía.
3.- Técnicas antirreflujo – Funduplicatura de Nissen
Se mantendrán los procinéticos y los bloqueantes H2 en el preoperatorio. Se utiliza la SNG de forma preoperatoria y la ISR.
Debe mantenerse el acceso a la cabeza para movilizar la sonda o los dilatadores esofágicos.
Bibliografía
1.- Sellick BA. The prevention of regurgitation during induction of anesthesia. Proceeding of the First European Congress of Anaesthesiology Vienna 1962; 1:89.
2.- EL-Orbany M, Connolly LA. Rapid sequence induction and intubation: current controversy. AnesthAnalg 2010; 110:1318““25. (PubMed)
3.- Benumof JL. Management of the difficult adult airway. With special emphasis on awake tracheal intubation. Anesthesiology 1991;75:1087““110. (PubMed)
4.- Salem MR. Anesthetic management of patients with“ a full stomach“. A critical review. AnesthAnalg 1970; 49:47““55. (PubMed)
5.- Stept WJ, Safar P. Rapid induction-intubation for prevention of gastric-content aspiration. Anesth Analg 1970; 49: 633““6. (PubMed)
6.- Vanner RG, Pryle BJ. Nasogastric tubes and cricoid pressure. Anaesthesia 1993; 48:1112““3. (PubMed)
Belén Cobo GarcíaEspecialista en Anestesiología y Reanimación
Hospital Universitario Fundación de Alcorcón. Madrid




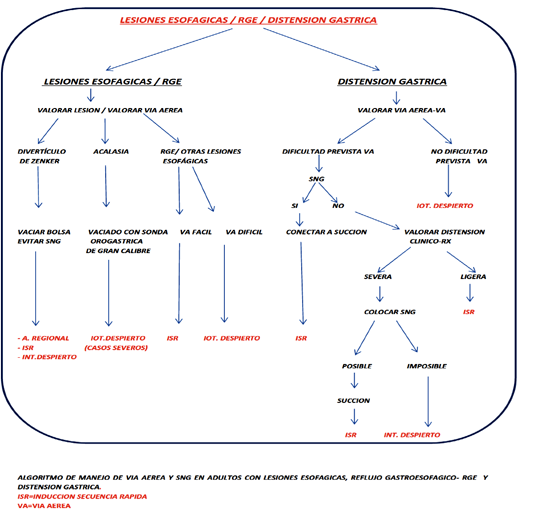
buenas noches, quiero felicitar a la Dra Belen Cobo por esta revisión, estuve viendo el articulo del Dr Ramez Salem y cols, por que me inquieto el algoritmo…: en la rama «distensión gástrica – valorar la vía aérea» están truncados las subdivisiones: si existe una dificultad prevista de la vía aérea el manejo debe ser con intubación despierto y si no hay esta dificultad si se pasa a SNG.
chau
excelente articulo