 Jose Miguel Marcos Vidal.
Jose Miguel Marcos Vidal.
Complejo Asistencial Universitario de León.
Artículos Referencia:
ESCMID guideline for the diagnosis and management of Candida diseases 2012: non-neutropenic patients. Clin Microbiol Infect 2012; 18 Suppl 7: 19-37. (PubMed) (pdf)
ESCMID guideline for the diagnosis and management of Candida diseases 2012: Diagnostic Procedures. Clin Microbiol Infect 2012; 18 Suppl 7: 9-18. (PubMed) (pdf)
“No hay un solo camino hacia la verdad en el campo de la medicina, porque la ciencia y el arte de la medicina están en un cambio continuo, pudiendo estar los datos publicados ya obsoletos en ese momento y su interpretación sesgada de manera involuntaria“.
Este es el párrafo de presentación de estas guías, que ya nos aconseja una interpretación prudente de las mismas, no siendo el objetivo de las mismas aportar verdades absolutas, sino ayudar al diagnóstico y tratamiento de la candidemia desde la perspectiva de la realidad que cada centro tiene.
En sus recomendaciones, estas guías han seguido los principios GRADE y AGREE, estableciendo grados de fuerza de recomendación graduados de la A a la D (Tabla 1).
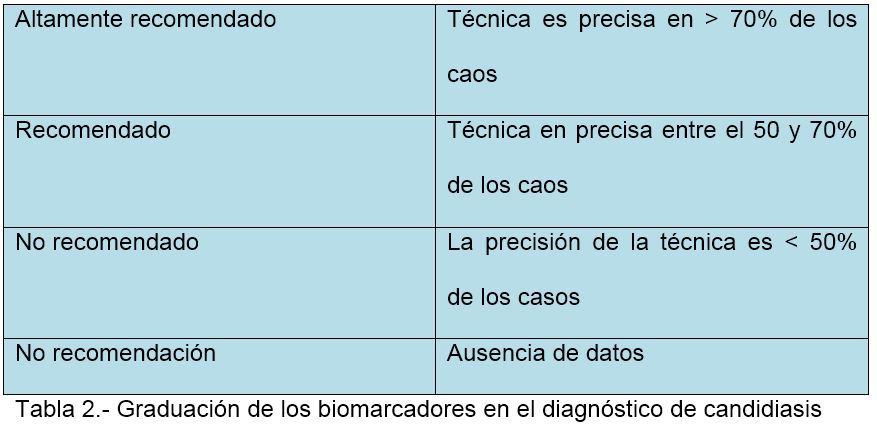
En la evaluación de los biomarcadores se utilizó una clasificación alternativa más adecuada que la anterior (Tabla 2).
Recomendaciones en el diagnóstico
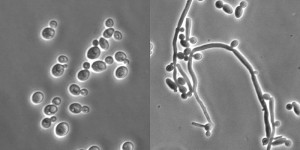
Candidemia
Para detectar la presencia de candida en sangre la prueba diagnóstica angular es el hemocultivo:
– Se recomienda la extracción de 3 hemocultivos, con un volumen de sangre total entre 40 y 60 ml.
– La técnica de elección es la venopunción, sin intervalo de tiempo entre las extracciones.
– El periodo de extracción debe ser diario si se sospecha candidemia, con una incubación de 5 días.
De esta forma la Sensibilidad del hemocultivo oscila entre el 50 y 75%, dejando claro que no es el método de elección para un diagnóstico precoz.
Como métodos de detección precoz se recomiendan el uso de biomarcadores (manano-anticuerpos antimanano y B-1,3-D, glucano), que adelantan la toma de decisiones diagnósticas 6 días respecto al hemocultivo.
Ambas presentan una Especificidad del 80%, tomando especial relevancia el resultado negativo de las mismas más que la positividad, ayudando a la toma de decisiones respecto a la retirada de un tratamiento ya iniciado.
Con los datos disponibles en la actualidad sobre el Septifast reconocen que no se pueden realizar recomendaciones.
Candidiasis invasiva
Se mantiene la recomendación de los hemocultivos, añadiendo el análisis histopatológico y cultivo de muestras de tejido, siempre que sea posible, reconociendo la dificultad en la obtención de muestras válidas.
Al igual que ocurre con el Septifast, la PCR sobre los tejidos o inmunohistoquímica son técncias actualmente con un aval insuficiente para su recomendación.
Tratamiento en el paciente no neutropénico
Profilaxis
Se establece un grado de recomendación B para el tratamiento con fluconazol en pacientes con dehiscencias repetidas y cirugía abdominal reciente.
“Tratamiento empírico para paciente con fiebre persistente y cultivos microbiológicos negativos, pero con riesgo de candidiasis invasiva“.
En la actualidad no se puede establecer ninguna recomendación de tratamiento en estos pacientes, aunque el tratamiento de una fungemia probable posiblemente se asocie a tasas mayores de supervivencia.
“Tratamiento preventivo en pacientes con evidencia microbiológiga de candidasis pero sin pruebas candidemia o candidiasis invasiva“.
Cuando se hace referencia a evidencia microbiológica se habla de la positividad del B-1,3-D.glucano, dando una grado de recomendación C al inicio del tratamiento antifúngico, dando muchas más importancia cómo se ha comentado antes a la negatividad del biomarcador. Se aborda también la positividad a cándida de muestras respiratorias, que no deben ser indicación de tratamiento antifúngico.
Tratamiento dirigido
Se establece nivel de recomendación A para las 3 equinocandinas, nivel B para la anfotericina B liposomal y voriconazol, y nivel C para el fluconazol, con excepción del tratamiento de la Candida parapsilosis en la que el fluconazol es superior a las equinocandinas.
Duración del tratamiento de la candidemia
Hasta 14 días después de la negativización de los hemocultivos, con toma de hemocultivos diaria. Si el paciente está estable se puede desescalar a fluconazol oral después de 10 días de tratamiento con equinocandina intravenoso.
Se debe descartar la endocarditis mediante ecocardiograma transesofágico y realizar fondo de ojo con periodicidad semanal para buscar corioretinitis o endoftalmitis. En el caso de catéter venoso pensar en fenómenos trombóticos.
Para todas estas recomendaciones se establecen nivel de recomendación B.
Candidemia relacionada con el catéter
Retirar el catéter, con un grado de recomendación A. Si no fuera posible, tratamiento con equinocandina o anfotericina B liposomal, con nivel de recomendación B.
Candidiasis ocular
Tratamiento con anfotericina B liposomal sola o combinada con flucitosina si la susceptibilidad de la especie es no conocida, en el caso de especies susceptinles a fluconazol o voriconazol tratar con estos (Grado de Recomendación A).
Se diferencia entre corioretinitis y endoftalmitis, precisando ésta último abordaje quirúrgico además de tratamiento farmacológico.
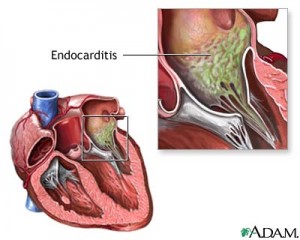
Endocarditis por Cándida
Tratamiento quirúrgico tanto sobre válvula nativa como protésica.
Sobre válvula nativa se describen tratamientos con caspofungina y anfotericina, ambos con o sin flucitosina.
En el caso de válvulas protésicas se emplean caspofungina o anfotericina B liposomal sin flucitosina, seguidos de tratamientos de larga duración con fluconazol.
Comentarios
En las Unidades de Cuidados Críticos el diagnóstico precoz de las infecciones por cándida continúa siendo un reto. Desde mi punto de vista como clínico estas guías aportan poco en nuestro día a día, teniendo en cuenta que siguen considerando como prioritarios los hemocultivos, que no son útiles para una toma de decisiones“ aguda“, dejando los biomarcadores (manano-anticuerpos antimanano y B-1,3-D.glucano) como herramientas útiles en este contexto.
Este contexto suele ser el de un paciente grave, con una infección intraabdominal, en el que iniciamos tratamiento empírico con antibioterapia de amplio espectro, y que además puede incluir un antifúngico. Tenemos pocas dudas de cómo desescalar ese tratamiento antibiótico, pero evidentemente no ocurre lo mismo con el tratamiento antifúngico. La presencia de manano-anticuerpos antimanano en nuestros hospitales es limitada, y recordar que el B-1,3-D.glucano no está disponible en España, así que resulta difícil adaptar las recomendaciones sobre biomarcadores a este entorno.
En estas guías siguen sin abordarse la utilidad de herramientas como el Candida Score, Ostrosky Candida Score, etc., recursos que los clínicos utilizamos en la toma de decisiones para este paciente“ tipo“ sobre el que iniciamos un tratamiento empírico.
Tanto las recomendaciones de las Guías IDSA cómo las que estamos abordando inciden en la indicación de equinocandina ante una candidemia o candidiasis invasiva, basándose en tasas de erradicación mayores en pacientes con valores de APACHE, disminuyendo además las interacciones medicamentosas, pero… ¿qué ocurre con nuestros tratamiento empírico?.
Coincidimos en que estamos realizando un“ sobretratamiento“, justificado por las cifras de mortalidad atribuible y directa de la candidemia, con tasa en nuestras Unidades de hasta un 20% de infección por Cándida. Y me surge la pregunta… ¿estas cifras son independientes de la duración del ingreso? En ningún momento en las guías se hace referencia a la historia del paciente, tiempo que lleva ingresado, factores de rieso, etc., apartado que como clínico también echo de menos.
En el apartado de profilaxis, se habla de tratamiento en cirugía abdominal con dehiscencias repetidas. ¿Este no es el tratamiento empírico qué los clínicos estamos haciendo? Resulta que para este indican el fluconazol, con un grado B, siendo la recomendación para la caspofungina C. Ante esto, mi pregunta es, ¿cuál es el lugar del fluconazol en este tratamiento empírico?, ¿son las interacciones farmacológicas las que lo limitan?, ¿estamos aumentando la supervivencia de nuestros pacientes con el sobretratamiento?
En el apartado de duración del tratamiento dirigido, establecen recomendación pero, nuevamente, echo a faltar algo en la toma de decisiones de mi día a día. ¿Cuándo retirar un tratamiento empírico?, ¿cuántos días debo sacar hemocultivos diarios ante la sospecha de una candidemia para, ante su negativización, retirar un tratamiento iniciado?
Después de leer estas nuevas guías, al igual que después de leer las de la IDSA, siguen sin resolverse mis dudas a nivel asistencial, considerando la ayuda de las mismas limitada a nivel asistencial, ya que dejan sin resolver un gran número de actuaciones en la mayoría e nuestro pacientes“ tipo“, sobre los que administramos tratamientos sin evidencia microbiológica. Así que el comentario de pasillo entre los clínicos sigue sin variar después de la aparcición de estas guías y es el… ¿cuándo aparecerá esa prueba diagnóstica rápida y fiable que, una vez que hemos“ puesto“, nos permita“ quitar“ en estas situaciones“ agudas“ el tratamiento?
Seguro que no está muy lejos… ahora esperar solo que también pueda estar disponible para todos.
Bibliografía
1.- Ullmann AJ, Cornely OA, Donnelly JP, Akova M, Arendrup MC, Arikan-Akdagli S, Bassetti M, Bille J, Calandra T, Castagnola E, Garbino J, Groll AH, Herbrecht R, Hope WW, Jensen HE, Kullberg BJ, Lass-Flí¶rl C, Lortholary O, Meersseman W, Petrikkos G, Richardson MD, Roilides E, Verweij PE, Viscoli C, Cuenca-Estrella M; ESCMID Fungal Infection Study Group. ESCMID* guideline for the diagnosis and management of Candida diseases 2012: developing European guidelines in clinical microbiology and infectious diseases. Clin Microbiol Infect. 2012 Dec;18 Suppl 7:1-8. (PubMed) (pdf)
2.- Cuenca-Estrella M, Verweij PE, Arendrup MC, Arikan-Akdagli S, Bille J, Donnelly JP, Jensen HE, Lass-Flí¶rl C, Richardson MD, Akova M, Bassetti M, Calandra T, Castagnola E, Cornely OA, Garbino J, Groll AH, Herbrecht R, Hope WW, Kullberg BJ, Lortholary O, Meersseman W, Petrikkos G, Roilides E, Viscoli C, Ullmann AJ; ESCMID Fungal Infection Study Group. ESCMID* guideline for the diagnosis and management of Candida diseases 2012: diagnostic procedures. Clin Microbiol Infect. 2012 Dec;18 Suppl 7:9-18. (PubMed) (pdf)
3.- Cornely OA, Bassetti M, Calandra T, Garbino J, Kullberg BJ, Lortholary O, Meersseman W, Akova M, Arendrup MC, Arikan-Akdagli S, Bille J, Castagnola E, Cuenca-Estrella M, Donnelly JP, Groll AH, Herbrecht R, Hope WW, Jensen HE, Lass-Flí¶rl C, Petrikkos G, Richardson MD, Roilides E, Verweij PE, Viscoli C, Ullmann AJ; ESCMID Fungal Infection Study Group. ESCMID* guideline for the diagnosis and management of Candida diseases 2012: non-neutropenic adult patients. Clin Microbiol Infect. 2012 Dec;18 Suppl 7:19-37. (PubMed) (pdf)
4.- Brozek JL, Akl EA, Compalati E et al. Grading quality of evidence andstrength of recommendations in clinical practice guidelines part 3 of 3. The GRADE approach to developing recommendations. Allergy 2011; 66: 588““595. (PubMed) (pdf)
5.- Brouwers MC, Kho ME, Browman GP et al. Development of theAGREE II, part 1: performance, usefulness and areas for improvement. CMAJ 2010; 182: 1045““1052. (PubMed) (pdf)
6.- Pappas PG, Kauffman CA, Andes D, Benjamin DK Jr, Calandra TF, Edwards JE Jr,Filler SG, Fisher JF, Kullberg BJ, Ostrosky-Zeichner L, Reboli AC, Rex JH, Walsh TJ, Sobel JD; Infectious Diseases Society of America. Clinical practice guidelines for the management of candidiasis: 2009 update by the Infectious Diseases Society of America. Clin Infect Dis. 2009 Mar 1;48(5):503-35. (PubMed) (pdf)
___________
El autor declara que el manuscrito no ha recibido financiación, que no existe conflicto de intereses que declarar y se han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes.
Jose Miguel Marcos Vidal. Médico Especialista en Anestesiología y Reanimación. Servicio Anestesiología, Reanimación y Terapeútica del Dolor. Complejo Asistencial Universitario de León.




1 Comment